

 更多“化学反应达平衡时,反应就停顿了,所以反应物的浓度与生成物的浓…”相关的问题
更多“化学反应达平衡时,反应就停顿了,所以反应物的浓度与生成物的浓…”相关的问题
温度为T的某抽空容器中,反应 达平衡时总压力为60kPa,则此反应的标准平衡常数Kθ=().
达平衡时总压力为60kPa,则此反应的标准平衡常数Kθ=().
nB=nB/nC=1,则此反应的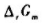 =();
=();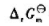 =();Kθ=().
=();Kθ=().
某一级对行反应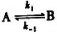 的速率常数、平衡常数与滥度的关系式分别为
的速率常数、平衡常数与滥度的关系式分别为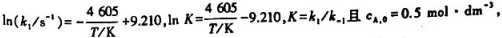
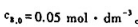 试计算:
试计算:
(1)逆反应的活化能;
(2)400K时,反应达平衡时的A,B的浓度CA.c,CB.c;
(3)400K时,反应10s时A,B的浓度CA,CB.
反应停对大小鼠剂量达4000mg/kg时几乎无致畸作用,而0.5~1.0mg/kg剂量即对人有致畸作用
A.实验动物的物种与毒效应
B.实验动物的品系与毒效应
C.实验动物的性别与毒效应
D.实验动物的年龄与毒效应
E.实验动物的生理营养状况与毒效应
A.升高温度使吉布斯自由能变和和标准吉布斯自由能变均增大
B.升高温度可以使平衡向右移动
C.升高温度可以使平衡常数增大
D.正反应自发时,随着反应进行,N2和H2分压逐渐减小,NH3分压逐渐增大,所以平衡常数Kp逐渐增大
将足量的固态氨基甲酸氨(NH2COONH4)放在抽空容器内恒温下发生分解反应并达平衡:

则此平衡系统的组分数C=().相数P=(),自由度F=().
N2O4按下式发生解离:
 已知52℃解离达平衡时有一半的N2O4发生解离,并知平衡系统的压力为100kPa。计算该反应的标准平衡常数。
已知52℃解离达平衡时有一半的N2O4发生解离,并知平衡系统的压力为100kPa。计算该反应的标准平衡常数。
当下述反应2SO2kg)+O2(g)=2SO3(g)达到平衡后,在反应系统中加入一定量的惰性气体,对于平衡系统有何影响?试就加入惰性气体后系统的体积保持不变或总压力保持不变这两种情况加以讨论。