

 更多“下列电池的电动势为0.981(V),试计算:的形成常数。”相关的问题
更多“下列电池的电动势为0.981(V),试计算:的形成常数。”相关的问题
有如下两个电池:
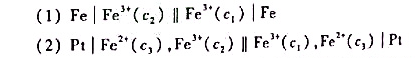
测得其电动势分别为E(1)和E(2),试求E(1)与E(2)之比。
下列电池的电动势为0.460V。计算反应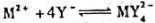 生成的配合物
生成的配合物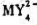 的稳定常数
的稳定常数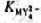 (已知
(已知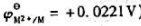 )。
)。
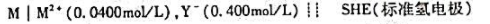
下列电池饱和 的电动势为-0.492V。计算HA的解离常数(不考虑液接电位,温度为25℃)。
的电动势为-0.492V。计算HA的解离常数(不考虑液接电位,温度为25℃)。
为测定下列吡啶与水之间的质子转移反应的平衡常数,
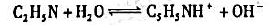
安装以下电池:
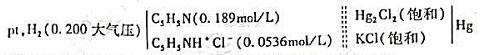
若25℃时电池电动势为0.563V,上述反应的平衡常数Kb为多少?
以Ag/AgC1与铜离子选择性电极组成下列电池饱和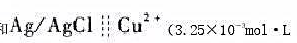
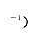 铜离子选择性电极
铜离子选择性电极
在25℃时,测得电池的电动势为0.124V。若用未知铜活度的溶液取代上述电池中Cu2+(3.25X10-3mo1•L-1)的溶液,测得其电动势为0.086V。计算未知液中pCu(不考虑液接电位)。
用下列电池按直接电位法测定草酸根离子浓度。
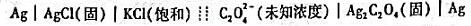
(1)推导出pC2O4与电池电动势之间的关系式
(2)若将一未知浓度的草酸钠溶液置入此电池,在25℃时测得电池电动势为0.402V,Ag-AgCl电极为负极,计算未知溶液的pC2O4。(已知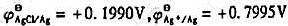 )
)
准确量取30.00ml弱酸HA,加水稀释至100ml,在下列电池中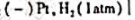
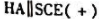 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
一原电池构成如下:
电极A:铜片插人2.0mol·dm-3CuSO4溶液和10mol·dm-3氨水的等体积混合溶液;
电极B:铜片插人1.0mol·dm-3CCuSO4溶液。
测得该电池的电动势E=0.39V,试求[Cu(NH3)4]2+的稳定常数。