

 更多“在稀醋酸溶液中,加入等物质量的固态NaAc,在混合溶液中不变…”相关的问题
更多“在稀醋酸溶液中,加入等物质量的固态NaAc,在混合溶液中不变…”相关的问题
在碘量瓶中加入5.00mL的NaClO漂白液(ρ=1.00gm·L-1),再加入过量的KI溶液.然后用稀H2SO4酸化,控制pH<9.立即以淀粉液为指示剂,用0.100mol.L-1Na2S2O3溶液滴定.到达终点时消耗Na2S2O3溶液体积为33.8mL.写出相关反应的离子方程式,并计算漂白液中NaClO的质量分数w(NaClO).
下列关于固体分散物的叙述哪一项是错误的()。
A.药物在固态溶液中是以分子状态分散的
B.共沉淀物中药物是以稳定晶型存在的
C.药物在简单低共熔混合物中仅以较细微的晶体形式分散于载体中
D.固体分散体也存在着某些缺点,例如储存过程中老化、溶出速度变慢等
E.固体分散体可以促进药物的溶出
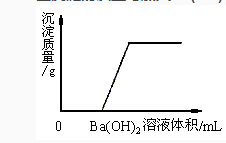
A.MgCl2和HCl
B.稀H2SO4和MgCl2
C.HCl和稀H2SO4
D.稀H2SO4和NaOH
简要回答下列问题:
(1)为什么金属Fe与盐酸反应生成Fe(Ⅱ),而与氯气反应生成Fe(Ⅲ)?
(2)向Pb2+的溶液中加入稀盐酸,然后过滤,测得滤液中仍有较多Pb(Ⅱ)。试解释其原因。
(3)为什么卤素互化物中卤素原子的数目经常是偶数,而碱金属多卤化物中卤素原子的数目却经常是奇数?
(4)氢氟酸在较稀的溶液中是完全解离的,但实测的Ka却为10-4数量级,属于弱酸。应如何解释?而浓的氢氟酸,其酸性较强。又应如何解释?
(5)常温下测得卤化氢气体对空气的相对密度是
HF 1.78;HCl 1.26;HBr 2.79;H 14.44。
由此计算出卤化氢的相对分子质量,HCI,HBr,HI均接近理论值,唯HF的相对分子质量与理论值20相差很大,试说明其原因。
(6)HClO,HClO2,HClO3,HClO4的酸性依次增强,试说明其原因。
(7)HClO,HClO3,HClO4的氧化性依次减弱,试说明其原因。
A.熔融法是制备固体分散体的方法之一,即将药物与载体的熔融物在搅拌情况下慢慢冷却
B.共沉淀物是由固体药物与载体二者以恰当比例而形成的非结晶性无定型物
C.固体分散体的类型有简单低共融混合物、固态溶液、共沉淀物
D.常用的固体分散技术有熔融法、溶剂法、溶剂一熔融法、研磨法等、
E.固体药物在载体中以分子状态分散时,称为固态溶液,此种情况药物的溶出最快
药物中氯化物杂质检查,是使该杂质在酸性溶液中与硝酸银试液作用生成氯化银浑浊液,所用的酸是
A.稀硫酸
B.稀醋酸
C.稀盐酸
D.稀硝酸
E.稀磷酸
药物中氯化物杂质检查,是使该杂质在酸性溶液中与硝酸银作用生成氯化物浑浊,所用的稀酸是()。
A.硫酸
B.硝酸
C.盐酸
D.醋酸
E.磷酸
药物中氯化物杂质检查,是使该杂质在酸性溶液中与硝酸银作用生成氯化物浑浊,所用的稀酸是
A.硫酸
B.硝酸
C.盐酸
D.醋酸
E.磷酸