 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
写出以下电池的电极反应、电池反应方程式,并计算电池电动热.(1)Zn|Zn2+(1×10-6mol·
写出以下电池的电极反应、电池反应方程式,并计算电池电动热.
(1)Zn|Zn2+(1×10-6mol·dm-3)||Cu2+(0.01mol·dm-3)|Cu
(2)Cu|Cu2+(0.01mol·dm-3)||Cu2+(2.0mol·dm-3)|Cu
(3)Pt,H2(1×105Pa)|HAc(0.1mol·dm-3)KCl(饱和),Hg2Cl2|Hg
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案



 更多“写出以下电池的电极反应、电池反应方程式,并计算电池电动热.(…”相关的问题
更多“写出以下电池的电极反应、电池反应方程式,并计算电池电动热.(…”相关的问题
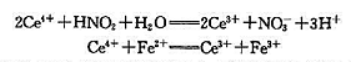
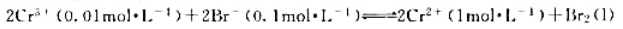
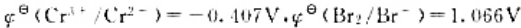
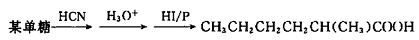

 ,增大体系中Cu2+的浓度必将使电池的电动势增大,根据电动势与平衡常数的关系可知,电池反应的
,增大体系中Cu2+的浓度必将使电池的电动势增大,根据电动势与平衡常数的关系可知,电池反应的 也必将增大。()此题为判断题(对,错)。
也必将增大。()此题为判断题(对,错)。
















