

 更多“ 对于可逆的等温等压反应,当与外界无有用功交换时,其自由焓的…”相关的问题
更多“ 对于可逆的等温等压反应,当与外界无有用功交换时,其自由焓的…”相关的问题
判断下列说法是否正确:
(1)在可逆过程中系统的熵值不变;
(2)如一个化学反应的ΔrH与温度无关,其ΔrS也与温度无关;
(3)根据dG=- SdT+ Vdp,对于任意等温等压过程dT=0, dp=0,则dG 一定为零;
(4)理想气体向真空膨胀△S= nRIn(V1/V2)
(5)在等温情况下,理想气体发生状态变化时,ΔP与ΔG相等;
(6)因为在等温等压下化学反应无论是否可逆,其反应热均等于过程中的SH,所以反应的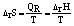
A.对在等温等压且不做非体积功的条件下,发生的各个化学反应过程和相变过程,可使用盖斯定律
B.对在等温等容且不做功的条件下,发生的各个化学反应过程,可使用盖斯定律
C.同一物质在盖斯定律涉及的几个反应中都出现时,只要无溶解等现象,相态不同也可加减
D.利用盖斯定律求某个反应的热效应时可引入一些别的反应,设想一些中间步骤,无论实际反应是否按这些中间步骤进行都可以
A.V2 > V’2
B.V2 = V’2
C.V2 < V’2
D.不确定