

 更多“反应A+B→C+D的速率方程为r=k[A][B],则反应()”相关的问题
更多“反应A+B→C+D的速率方程为r=k[A][B],则反应()”相关的问题
对于符合质量作用定律的化学反应 其速率方程为
其速率方程为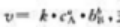 式中k称为(),CA和CB分别表示(),a+b称为()。
式中k称为(),CA和CB分别表示(),a+b称为()。
溶液反应的速率方程为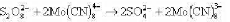 20°C,反应开始时只有两反应物,其初始浓度依次为0.01mol·dm-3,0.02mol·dm-3,反应20h后,测得
20°C,反应开始时只有两反应物,其初始浓度依次为0.01mol·dm-3,0.02mol·dm-3,反应20h后,测得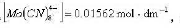 求k。
求k。
A.r=kc(NO2)2
B.r=kc(NO2)c(CO)
C.r=kc2(NO2)c(CO)
D.r=kc(CO)
A.该反应一定是基元反应
B.该反应一定是复合反应
C.该反应为二级反应
D.该反应为双分子反应
(1)若初始浓度CA.o=0.02mol.dm-3.CB.O=0.04mol·dm-3,水t1/2;
(2)若将过敢的挥发性固体反应物A与B装入sdm3密闭容器中,问25℃时0.5mol转化为产物需多长时间?(已知25℃时A和B的饱和熊气压分别为10kPa和2kPa)
A.b(b+d)/n
B.(c+d)(a+b)/n
C.(b+d)(a+b)/n
D.(b+d)(c+d)/n
E.d(b+d)/n
有人对反应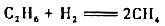 提出如下机理:
提出如下机理:
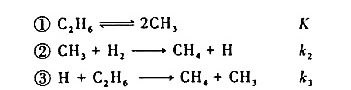
试用稳态近似法和平衡假设法推导生成CH4的速率方程微分表达式,并用已知数据K,k2,k3表示速率常数k。
2NO2(g).25℃下该反应的初始速率实验数据如表3-1:

(1)写出反应速率方程;
(2)计算25℃时反应速度系数k;
(3)co(NO)=0.0030mol·L-2,co(O2)=0.0015rmol·L-2时,相应的初始速半为多少?
A.|A+B|=|A|+|B|
B.|kA|=k|A|
C.r(A+B)=r(A)+r(B)
D.r(kA)=r(A)