

 更多“以0.1000mol·L-1Na2S2O3溶液滴定20.00…”相关的问题
更多“以0.1000mol·L-1Na2S2O3溶液滴定20.00…”相关的问题
A.0.1000mol/LHCI
B.0.1000mol/LHAc
C.0.01000molLHCI
D.0.01000mol/LHAc
用C(NaOH)0.1000mol/L的NaOH溶液滴定C(H2SO4)0.1000mol/LH2SO4溶液20.00ml,以甲基红为指示剂,问终点时需要消耗NaOH溶液多少毫升?
用0.1000mol/LHCl溶液滴定0.1000mol/LNa2CO3溶液至pH5.00。计算有百分之几的Na2CO3变成了H2CO3?剩下的主要组分是什么?如果煮沸溶液以除尽CO2,冷却后溶液的pH为多少?(H2CO3的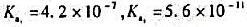 )
)
称取某弱酸HA试样1.0264g,溶于适量水中,以酚酞为指示剂,用0.1000mol/LNaOH滴定,当滴定剂加到10.50mL时,溶液的pH为4.20;滴定至终点时,消耗NaOH溶液24.70mL。求:

有一混合碱样品含Na2CO3、NaHCO3与NaOH三者中的两种。现称取样品0.2906g,以酚酞作指示剂,滴定用去0.1000mol·L-1HCl标准溶液28.60mL,再加入甲基橙指示剂又消耗24.10mL,问样品中含有何组分,其各自的百分含量是多少?
A.以上指示剂均不可
B.酚酞
C.中性红(变色范围pH6.8~8.0)
D.铬黑T
E.A和B均可
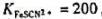
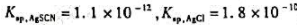 )
)
准确量取30.00ml弱酸HA,加水稀释至100ml,在下列电池中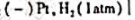
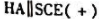 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。