

 更多“用下列物质标定HCI溶液浓度:(1)在1100C烘过的Na2…”相关的问题
更多“用下列物质标定HCI溶液浓度:(1)在1100C烘过的Na2…”相关的问题
响)?
(1)滴定速度太快,附在滴定管壁上的盐酸来不及流下来就读取滴定体积;
(2)称取Na2CO3时,实际质量为0.1238g,记录时误记为0.1248g;
(3)在将盐酸标准溶液倒入滴定管之前,没有用盐酸淋洗滴定管;
(4)使用的Na2CO3中含有少量的NaHCO3。
两者均保存妥当,则选()作为基准物质更好,原因为().若Na2CO,吸水,则标定结果();若硼砂结晶水部分失去,则标定结果()(以上两项填“无影响”、“偏高”或“偏低”).
下列情况将对分析结果产生何种影响? A.正误差,B.负误差,C.无影响,D.结果混乱。
(1)标定HCl溶液浓度时,使用的基准物Na2CO3中含有少量NaHCO3
(2)未按操作规程等待,刚滴定完,附在管壁的滴定剂还未流下来就读数了;
(3)配制滴定剂时经过加热溶解,在进行标定的过程中,滴定剂未经完全冷却就装入滴定管中(已经润洗)开始滴定
(4)配制标准溶液时未将容量瓶内溶液福匀
(5)用移液管移取试样溶液时,事先来用待移取溶液润沈移液管
(6)称量时,承按试样的锥形瓶潮湿
(7)溶解称量于维形瓶中的基准物质时,加水的体积有多有少
(8)用酸式消定管进行躏定中,发现旋塞处滞液
(9)滴定过程中不怕在酒定管中引入了气泡,读数时未发现。
(10)滴定管内壁有油污,滴定结束后管内壁挂有液珠。
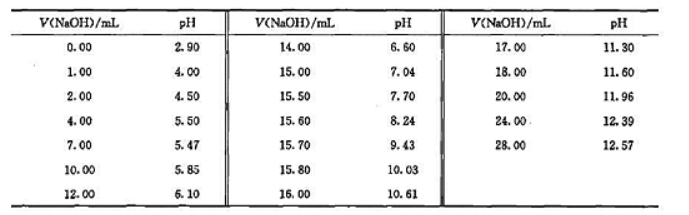
(1)绘制pH-V(NaOH)的曲线,从曲线的拐点确定测定终点.
(2)绘制ΔpH-V(NaOH)的曲线,从曲线的最高点确定测定终点.
(3)用二次微商计算法,从曲线的最高点确定滴定终点.
(4)根据(3)的值计算HCI的浓度.
下列几种化学试剂均为实验室常用试剂,分别计算它们的物质的量浓度和质丹摩尔浓度.
(1)浓盐酸,含HCI 37.0%,密度1.19 g·cm-1;(2)浓硫酸,含H2SO4,98.0%,密度1.84g·cm-3;(3)浓硝酸,含HNO370.0%,密度1.42 g·cm-3;(4)浓氨水,含NH328.0%,密度0.90 g·cm-3。
A.偏低
B.偏高
C.无影响
D.不确定
(1)每升碱液吸收了多少克CO2?
(2)用该碱液滴定某一元弱酸,若浓度仍以0.1026ml·L-1计算,会引起多大误差?