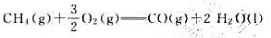更多“PCl5(g)的分解反应是PCl5(g)====PCl3(g…”相关的问题
更多“PCl5(g)的分解反应是PCl5(g)====PCl3(g…”相关的问题
A.吸热
B.放热
C.没有热效应
D.无法确定
PCl5的分解反应为
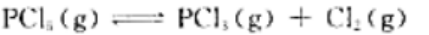 升高温度时,PCl5的分解百分率增大。试回答下列问题:
升高温度时,PCl5的分解百分率增大。试回答下列问题:
(1)PCl5分解反应是吸热反应还是放热反应?
(2)在恒温时,缩小反应容器的体积增大压力,PCl5分解百分率有何影响?
A.在298K时,H2O(1)和H2O(g)共存
B.S(s),S(I)和S(g)平衡
C.C2HsOH(I)和H2O(1)的混合物
D.一定量的PCl5(g)分解平衡时,PCl5(g)=PCl3(g)+Cl2(g)
在523.15K时,将0.70molPCl5(g)置于2.0L密闭容器中,待其达到平衡
PCl5(g) PCl3(g)+Cl2(g)经测定PCl5(g)的物质的量为0.20mol。
PCl3(g)+Cl2(g)经测定PCl5(g)的物质的量为0.20mol。
(1)求该反应的标准平衡常数KΘ及PCl5(g)的平衡转化率α。
(2)在上述平衡系统中再加入0.10mol PCl5(g),求重新达平衡后各物质的平衡分压。
温度T时,将PCl5(g)通入一密闭容器中,发生下列反应: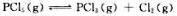 平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数
平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数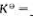 ().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
某温度下,反应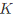 的平衡常数
的平衡常数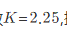 。把一定量的PCl5引入一真空瓶内,达平衡后PCl5的分压为2.533×104Pa,则PCl3的分压是______Pa,PCl5的解离分数______。
。把一定量的PCl5引入一真空瓶内,达平衡后PCl5的分压为2.533×104Pa,则PCl3的分压是______Pa,PCl5的解离分数______。
A.CH4(l)+2O2(g)=COg(g)+2H2O(g)
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g)
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l)
D.