

 更多“在氯化钡溶液中滴加某种溶液,生成白色沉淀。下列说法中错误的是…”相关的问题
更多“在氯化钡溶液中滴加某种溶液,生成白色沉淀。下列说法中错误的是…”相关的问题
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
A.在Ca(OH)2溶液中加入稀盐酸,无明显变化
B.在NaOH溶液中通入CO2气体,有白色沉淀生成
C.在Ca(OH)2溶液中滴加石蕊溶液,溶液呈蓝色
D.在NaOH溶液中加入CuSO4溶液,有蓝色沉淀生成
推理判断:
(1)无色晶体(A)易溶于水,向其水溶液中滴加氯水,溶液变黄有(B)生成:继续滴加氯水时,黄色消失有(C)生成。向(A)的水溶液中滴加高氯酸生成白色难溶物(D)。向(B)的水溶液中滴加二氯化铁时有(E)生成,(E)与硫氰化钾溶液作用,有红色物质生成。向(C)的水溶液中加入(A),酸化后有(B)生成。
试给出(A),(B),(C),(D)和(E)的化学式,并完成各步反应的离子反应式。
(2)白色粉末是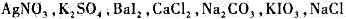 中某两种的混合物。该粉末加到水中形成白色沉淀,再加入稀硝酸酸化时白色沉淀消失且溶液发黄,再将溶液微热一段时间后滴加氨水至碱性,又形成白色沉淀且溶液变清。
中某两种的混合物。该粉末加到水中形成白色沉淀,再加入稀硝酸酸化时白色沉淀消失且溶液发黄,再将溶液微热一段时间后滴加氨水至碱性,又形成白色沉淀且溶液变清。
试判断原白色粉末的组成,说明理由并写出相关反应的方程式。
A.某无色溶液中滴加酚酞试液,溶液不变色,则该溶液一定是酸性溶液
B.某物质中滴加稀盐酸,生成无色气体,证明该物质中一定含CO32-
C.某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则该溶液中一定含有SO42-
D.某无色溶液中滴加NaOH溶液后加热,生成使湿润的红色石蕊试纸变蓝的气体,证明该溶液中一定含有NH4+
A.在稀硫酸溶液中显蓝色荧光
B.在稀氢氧化钠溶液中显蓝色荧光
C.在微酸性水溶液中加溴试液和氨溶液即显翠绿色
D.加入硫酸铜试液和20%的氢氧化钠溶液,显蓝紫色
E.加入氯化钡试液,即生成白色沉淀;分离,沉淀在盐酸和硝酸中均不溶解
A.在稀硫酸溶液中显蓝色荧光
B.在稀氢氧化钠溶液中显蓝色荧光
C.在微酸性水溶液中加溴试液和氨溶液即显翠绿色
D.加入硫酸铜试液和20%的氢氧化钠溶液,显蓝紫色
E.加入氯化钡试液,即生成白色沉淀;分离,沉淀在盐酸和硝酸中均不溶解
A.盐酸普鲁卡因
B.异戊巴比妥
C.地西泮
D.咖啡因
E.四环素
放出,同时溶液中有白色沉淀(C)析出。(C)在空气中迅速变为灰绿色,黑色,最后变为红棕色沉淀(D)。(D)溶于稀盐酸中生成棕黄色溶液(E)。向溶液(E)中滴加KI溶液,先有褐色沉淀(F)析出,随后变为红棕色溶液(G)。若在滴加KI溶液之前先加入过量KF溶液,则无此现象。向(D)的浓NaOH悬浮液中通入氯气,可得到紫红色溶液(H)。在(A)溶液和(H)溶液中分别滴加BaCl2溶液,均可析出沉淀,但前者是白色沉淀(I),后者是紫红色沉淀(J)。沉淀(I)不溶于HNO3,但(J)遇HNO3即分解并放出(K)。试给出(A),(B),(C),(D),(E),(F),(G),(H),(I),(J)和(K)所代表的物质的化学式,并用化学反应方程式表示各过程。