

 更多“写出下列各电池的电池反应。计算25°C时各电池的电动势、各电…”相关的问题
更多“写出下列各电池的电池反应。计算25°C时各电池的电动势、各电…”相关的问题
IZn)=-0.7620V.E-[CI-IAgCl(s)IAgI=0.2222V.电池电动势的温度系数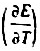 =-4.02x10-4V·K-1.
=-4.02x10-4V·K-1.
(1)写出电池反应;
(2)计算反应的标准平衡常数Kθ;
(3)计算电池反应可逆热Qr,m;
(4)求溶液中ZnCl2的平均离子活度因子ya.
已知铅酸蓄电池
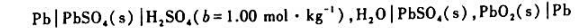
在25°C时的电动势E=1.9283V,Eθ=2.0501V.该电池的电池反应为
Pb(s)+PbO2(s)+2SO42-+4H+→2PbSO4(s)+2H2O
(1)请写出该电池的电极反应;
(2)计算该电池中硫酸溶液的活度a、平均离子活度az及平均离子活度因子γz;
(3) 已知该电池的温度系数为5.664x10-5V·K-1,计算电池反应的ΔrGm,ΔrSm,ΔrHm,
及可逆热Qr,m.
丙烷燃料电池的电极反应为
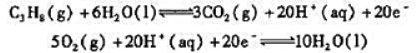
(1)指出正极反应和负极反应;
(2)写出电池反应方程式;
(3)计算25℃下丙烷燃料电池的标准电动势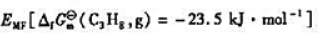
根据下列反应组成电池
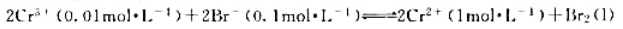
(1)写出电池符号;
(2)计算298K时的电动势,并判断反应自发进行的方向;
已知
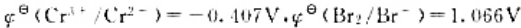
浓差电池
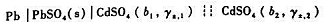
|PbSO4(s)|Pb,其中b1=0.2mol·kg-1.ya.1=0.1;b2=0.02mol·kg-1.Ya.z=0.32.已知在两液体接界处Cd2+的迁移数的平均值为t(Cd2+)=0.37.
(1)写出电池反应:
(2)计算25℃时液体接界电势E(液接)及电池电动势E.
(1)写出电池反应方程式;
(2)由附表六查得Eθ(Cl2/Cl-),计算E(Co2+/Co);
(3)p(Cl2)增大时,电池的电动势将如何变化?
(4)当CO2+浓度为0.010mol·L-1其他条件不变时,电池的电动势是多少伏?
甲烷燃烧过程可设计成燃料电池.当电解质为酸性溶液时,电极反应和电池反应分别为
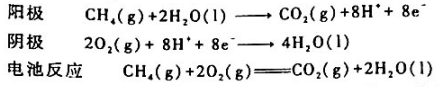
已知,25°C时有关物质的标准摩尔生成吉布斯函数 为
为
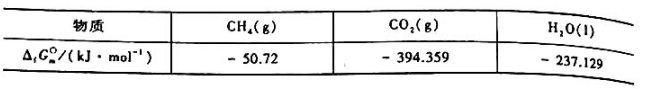
计算25°C时该电池的标准电动势.
325kPa).
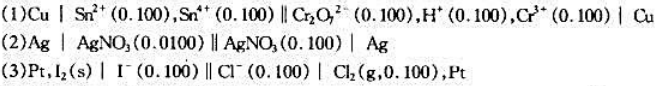
写出以下电池的电极反应、电池反应方程式,并计算电池电动热.
(1)Zn|Zn2+(1×10-6mol·dm-3)||Cu2+(0.01mol·dm-3)|Cu
(2)Cu|Cu2+(0.01mol·dm-3)||Cu2+(2.0mol·dm-3)|Cu
(3)Pt,H2(1×105Pa)|HAc(0.1mol·dm-3)KCl(饱和),Hg2Cl2|Hg
铅酸著电池的电极反应为
负极: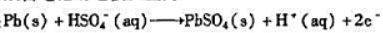
正极: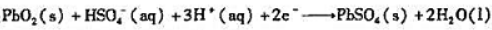
(1)计算铅酸费电池的标准电动势.
(2)如果将6个(1)中的铅酸蓄电池串连在一起,其总电动势为多少?
(3)充电时的电极反应如何?写出相应的反应方程式.
(4)在使用过程中,可用测定硫酸密度的方法,确定铅酸蓄电池是否需要充电,这是什么道理?
(5)充电时,需要用新的浓度大的硫酸咎换电池中的稀硫酸吗?为什么?